Как выбрать центрифугу для A-PRF и i-PRF
- 29 марта 2018
- Просмотров: 11707
Почему мы выбираем новые методы. Одна из причин — неудовлетворенность от обещаний различных фирм, производящих материалы. Каждый хирург сталкивался с явлением, когда при открытии места с ранее проведенной аугментацией вместо костной ткани мы видим мягкий белый порошок. Чудо происходит не всегда, хотя производители уверяют нас в обратном.
Экономическая составляющая также влияет на нашу работу. Девальвация национальной валюты, когда в два раза увеличивается расход и снижается рентабельность на фоне снижения общей покупательной способности.
Данные явления служат толчком для применения новых методик.
В данной статье хотелось бы подробнее разобрать использование A-PRF и i-PRF.
Методика не новая, но усовершенствованная. Центрифугирование крови пациента с образованием обогащенной тромбоцитами плазмы (БоТП) широко применяется в стоматологии и смежных специальностях уже продолжительное время.
И в то же время существует определенная неразбериха. Многие доктора центрифугируют кровь, при этом получая не совсем то, что нужно. Попробуем разобраться.
В чем отличие БоТП от PRF
Аббревиатура PRF переводится как Platelets Reach Fibrin (богатый тромбоцитами фибрин). Приставка A-PRF означает advance, то есть «улучшенный». Приставка i-PRF никак не переводится, появилась, скорее всего, после всеобщей «i-мании»: по сути, это жидкость, используемая для склеивания остеопластического материала.
PRP — Platelets Reach Plasma — богатая тромбоцитами плазма, то же самое, что и БоТП.
PRGF — Platelets Reach Growth Factors — обогащенная факторами роста плазма.
Упрощенный механизм заживления выглядит так:
Повреждение — кровотечение — свертывание крови — образование сгустка — выделение факторов роста из тромбоцитов и лейкоцитов — образование кровеносных сосудов — заживление раны. PDGF, TGF, IGF, VEGF, BMP и др. — все эти факторы роста находятся в тромбоцитах и лейкоцитах. Они обеспечивают заживление. Из одной и той же пробирки при центрифугировании мы можем получить PRF, PRP, PRGF. При этом образование полноценного сгустка происходит только при получении PRF.
Почему это важно? Потому что факторы роста могут выделиться у тромбоцитов только после образования сгустка (Сhoukroun, 2001). Также фибрин является матрицей для деления клеток и образования новых сосудов (Donan, Gasling, 2010). Это ключевой момент отличия PRF от PRP и PRGF.
PRF содержит: тромбоциты — 100 %, лейкоциты — 60 %, естественный фибрин.
Кроме того, содержание лейкоцитов в PRF — 65 %, PRP — 50 %, PRGF — 0 %. Напомним, что лейкоциты также обеспечивают образование факторов роста.
Далее определим различия по скорости высвобождения факторов роста.
PRP — все высвобождаются сразу. PRGF — нет данных. PRF — в течение 7 суток. То есть высвобождение факторов роста из PRF идет по принципу «капля за каплей» в течение 7 дней. Так как время действия факторов роста равно 3 минутам, эффект кратковременен. Отсюда можно сделать вывод, что их концентрация при получении PRF будет постоянной в течение 7 суток.
Поэтому, если мы хотим получить PRF, а не PRP или PRGF, крайне важно соблюдать протокол.
Если этого не делать, полноценного PRF не получается. Один и тот же пациент и три разных результата. Основное отличие — размер.
Какую выбрать центрифугу?
Существуют разные. Самый важный момент — поддержка постоянной температуры. К примеру, центрифуга фирмы Salvin разогревает сгусток до 45 градусов через 8 минут. EBA, наоборот, снижает температуру до 21 градуса. Medifuge снижает температуру до 18 градусов. Специализированная центрифуга под PRF держит температуру постоянной — 28—29 градусов, тем самым обеспечивая образование максимального по величине сгустка (Сhoukroun, 2010).
На своем опыте мы проверили, что для получения полноценной PRF подходят только специализированные центрифуги. В других PRF или не получается, или получается очень малого размера!
Конечно, на процесс образования фибринового сгустка влияют и общие факторы. Это лейкоцитоз, изменение гормонального фона, диета, вредные привычки (курение).
Также хотелось бы обратить внимание на PRF — экссудат, который образуется после получения аутогенной мембраны. Он содержит плазму и адгезивные белки (фибронектин и витронектин). Как его нужно использовать? Любой графт рекомендуется замешивать с использованием этой жидкости и кусочков полученной мембраны (Сhoukroun, 2009). Это обеспечивает мощный потенциал биосовместимости материала.
Общие принципы образования PRF:
-
Центрифугирование без антикоагулянтов в специальных пробирках A-PRF.
-
Образование сгустка происходит физиологично.
-
Образуется строго определенный продукт.
-
В конце центрифугирования мы имеем сгусток и факторы роста (из лейкоцитов и тромбоцитов).
-
Для образования A-PRF скорость равна 1300 об./мин., время — 8 мин.
-
Для образования i-PRF скорость равна 700 об./мин., время — 3 мин.
Теперь на клинических примерах покажем использование A-PRF и i-PRF.
В клинику обратился пациент с адентией на верхней челюсти. Планируется увеличение толщины альвеолярного отростка во фронтальной области с использованием костных блоков, открытый синус-лифтинг с двух сторон. Получено 12 пробирок A-PRF (рис. 1).
|
Рис. 1. Получено 12 пробирок A-PRF. |
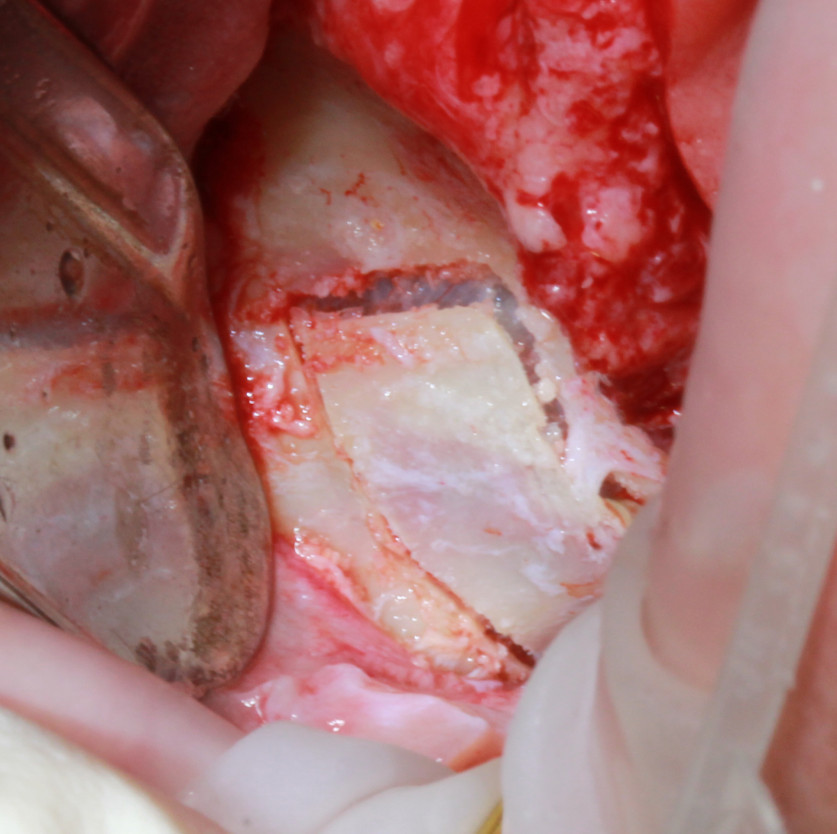
Вид после A-PRF-бокса. Костнопластический материал смешивается с кусочками A-PRF-мембраны и экссудата, полученными из PRF-бокса (рис. 2). С помощью пьезохирургии создается прямоугольной формы доступ для открытого синус-лифтинга (рис. 3).
|
Рис. 2. Костнопластический материал смешивается с кусочками A-PRF-мембраны и экссудата, полученными из PRF-бокса. |
Рис. 3. С помощью пьезохирургии создается прямоугольной формы доступ для открытого синус-лифтинга. |
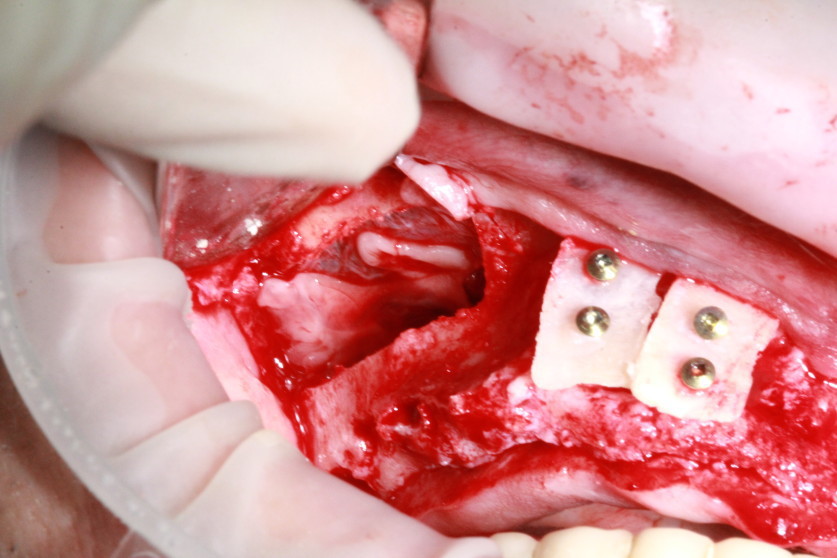
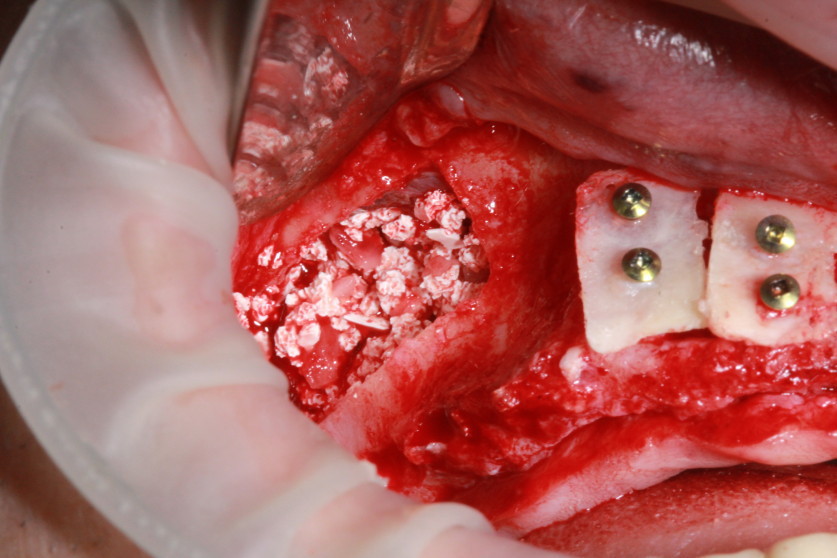
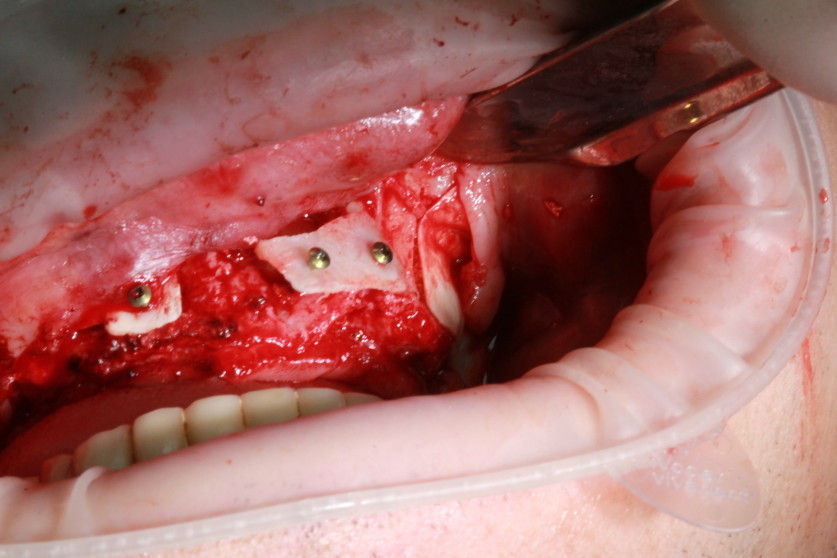
После аккуратного извлечения этот костный блок делится на две части для использования во фронтальной области. Для создания нового дна гайморовой пазухи используем две мембраны A-PRF, вносится материал (рис. 4, 5).
|
Рис. 4. Для создания нового дна гайморовой пазухи используем две мембраны A-PRF, вносится материал. |
Рис. 5. Для создания нового дна гайморовой пазухи используем две мембраны A-PRF, вносится материал. |
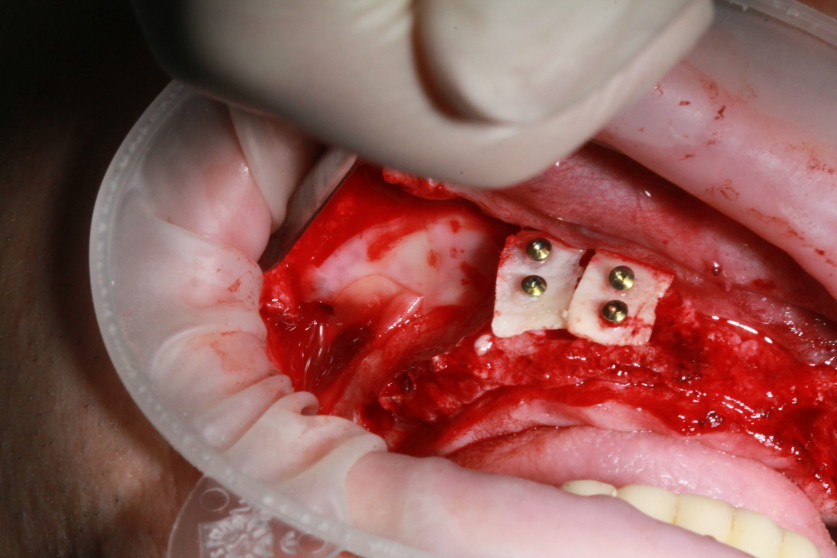
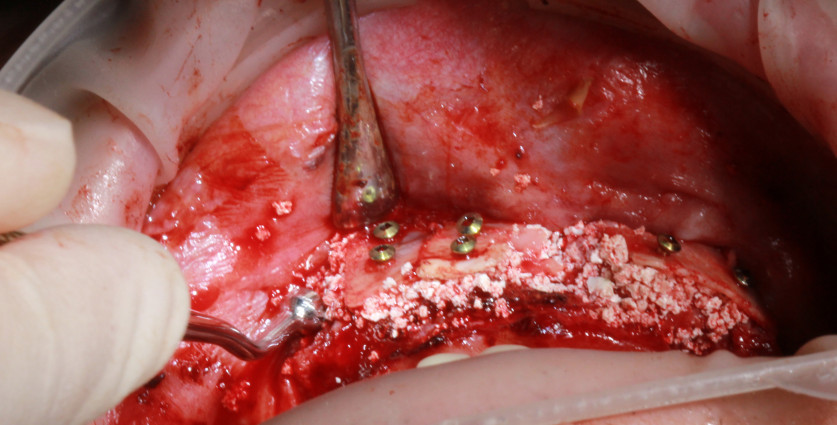
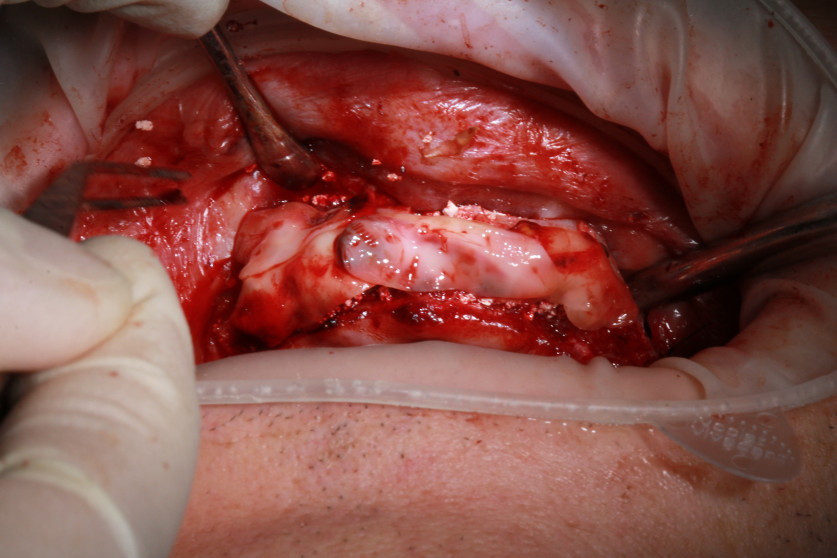
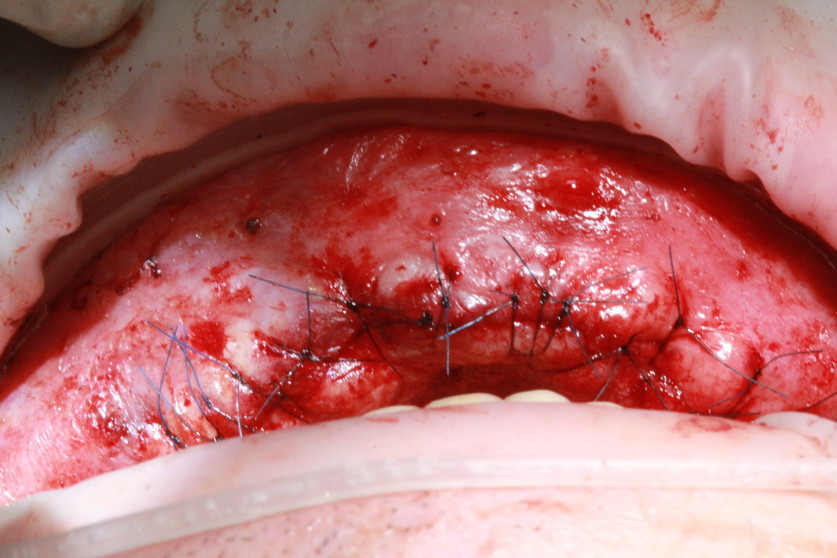
Для закрытия окна используем также две мембраны A-PRF (рис. 6). Аналогичные действия производятся и с правой стороны (рис. 7). Костные блоки закрываются A-PRF-мембранами (рис. 8, 9). Рана ушита без натяжения (рис. 10).
|
Рис. 6. Для закрытия окна используем также две мембраны A-PRF. |
Рис. 7. Аналогичные действия производятся с правой стороны. |
Рис. 8. Костные блоки закрываются A-PRF-мембранами. |
|
Рис. 9. Костные блоки закрываются A-PRF-мембранами. |
Рис. 10. Рана ушита без натяжения. |
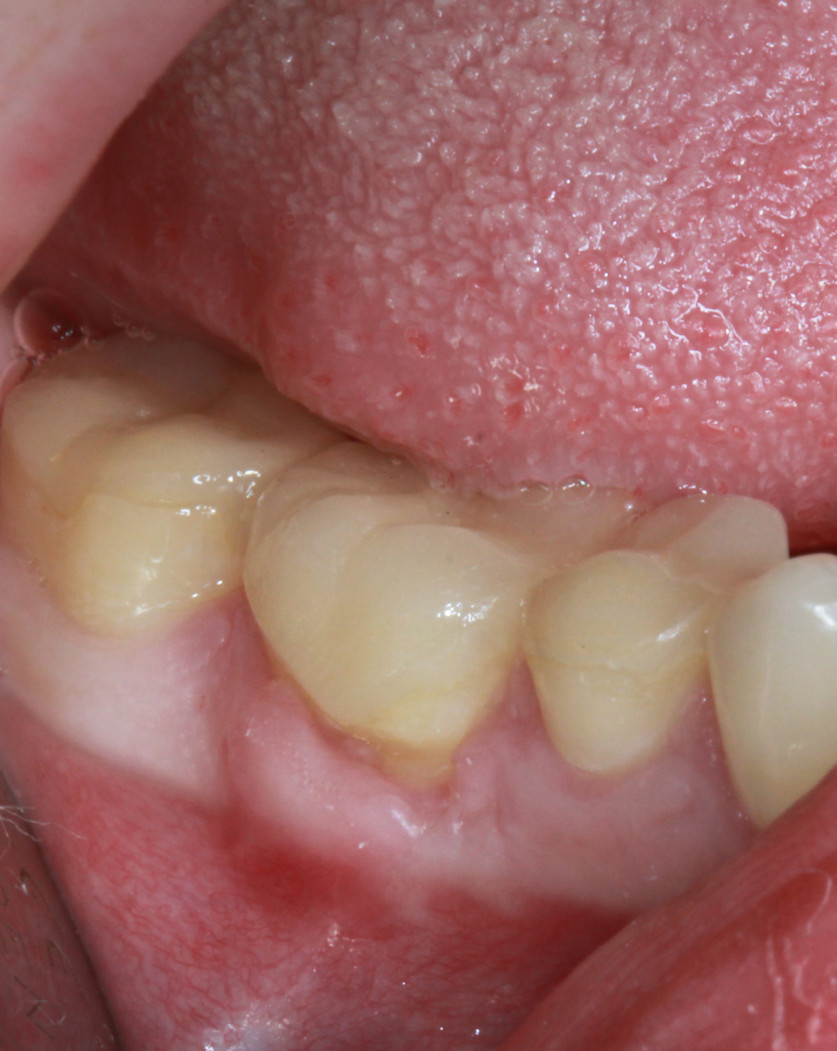
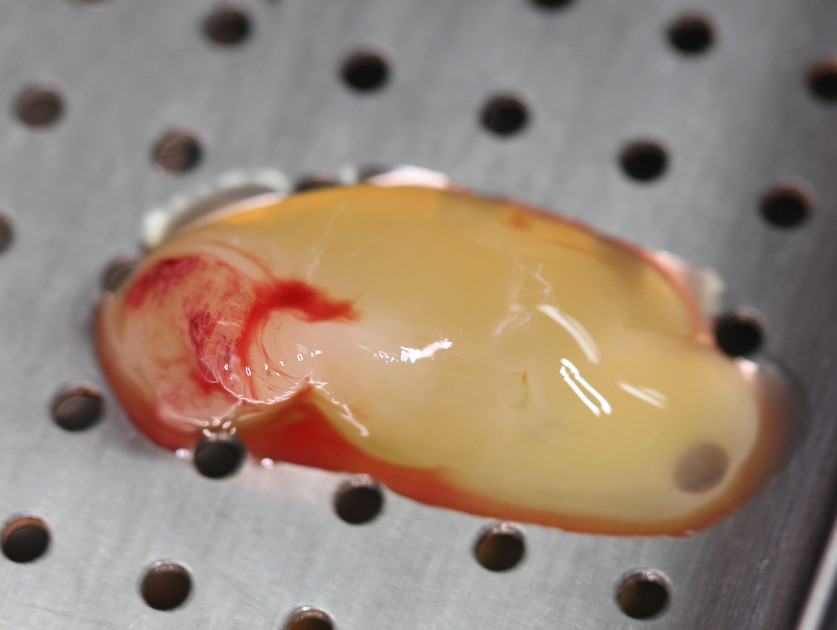
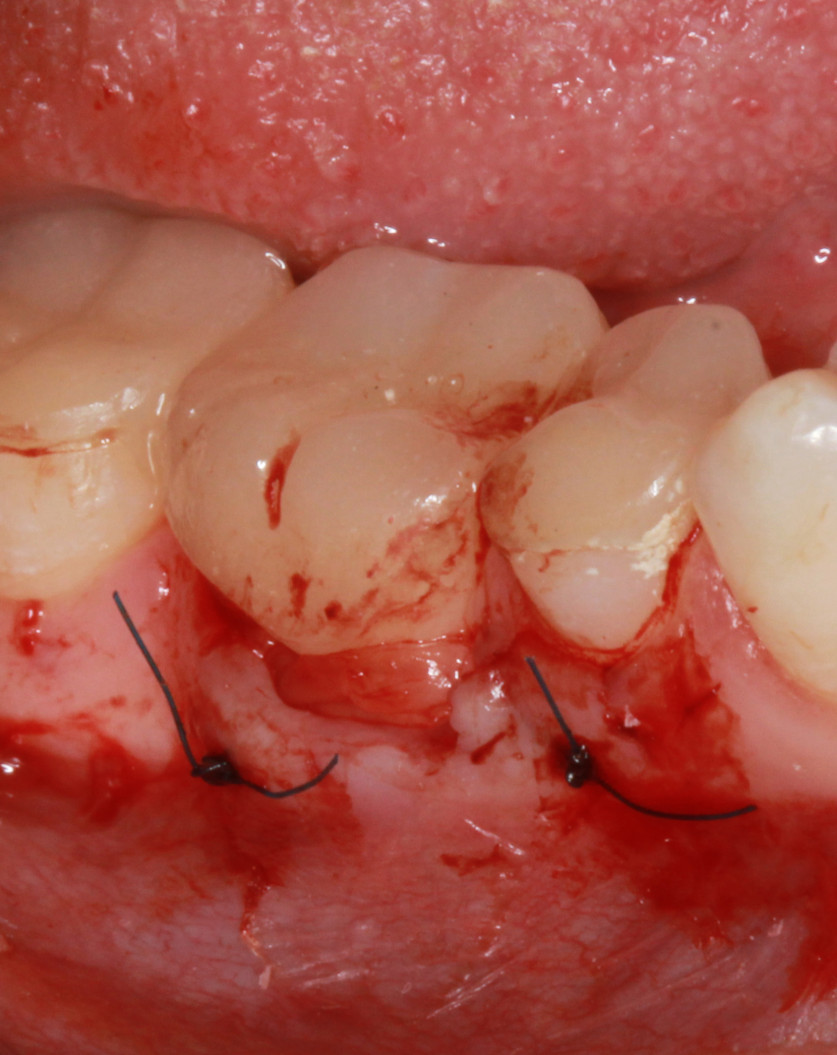
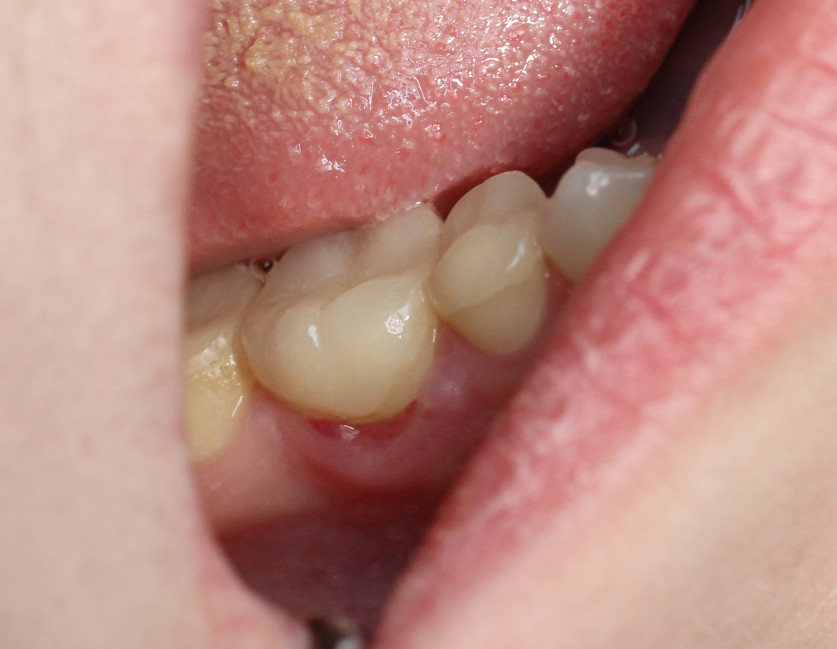
Очень практично использовать A-PRF для закрытия рецессии десны. В клинику обратилась пациентка с жалобами на боли от холодных раздражителей в области шейки 46 зуба (рис. 11). Принято решение о закрытии зоны рецессии с использованием трансплантата, полученного по технологии A-PRF. Это даст минимизацию операционной травмы, отсутствие болей в области неба в послеоперационном периоде, повысит общий комфорт пациента. После центрифугирования и отжимания получена A-PRF-мембрана (рис. 12, 13). Создан идеальный по размеру трансплантат. После создания конверта трансплантат уложен на место (рис. 14). Вид через три недели (рис. 15).
|
Рис. 11. Клиническая картина до лечения. |
Рис. 12. После центрифугирования и отжимания получена A-PRF-мембрана. |
Рис. 13. После центрифугирования и отжимания получена A-PRF-мембрана. |
|
Рис. 14. После создания конверта трансплантат уложен на место. |
Рис. 15. Вид через три недели |
Резюмируем показания к применению A-PRF.
Итак, A-PRF можно использовать:
- В качестве мембраны (период резорбции 1—1,5 месяца) при костной пластике.
- При закрытии перфораций при открытом синус-лифтинге.
- В качестве остеопластического материала при синус-лифтинге.
- При пластике мягких тканей как соединительнотканный трансплантат.
- Для сохранения костной ткани в лунках после удаления зубов.
- Для профилактики альвеолитов.
- Для обеспечения быстрейшего заживления и образования костной ткани за счет стимуляции ангиогенеза.
- Для снижения общего количества осложнений за счет стимуляции процессов регенерации.
- Для существенного снижения себестоимости костной пластики.
- Самое главное — замена любых искусственных мембран и получение биосовместимой аутогенной мембраны с очень низкой себестоимостью (порядка 2 долларов).
Д. В. Коротких, главный врач СК «Дент и К»
А. А. Парфенова, врач-стоматолог СК «Дент и К»